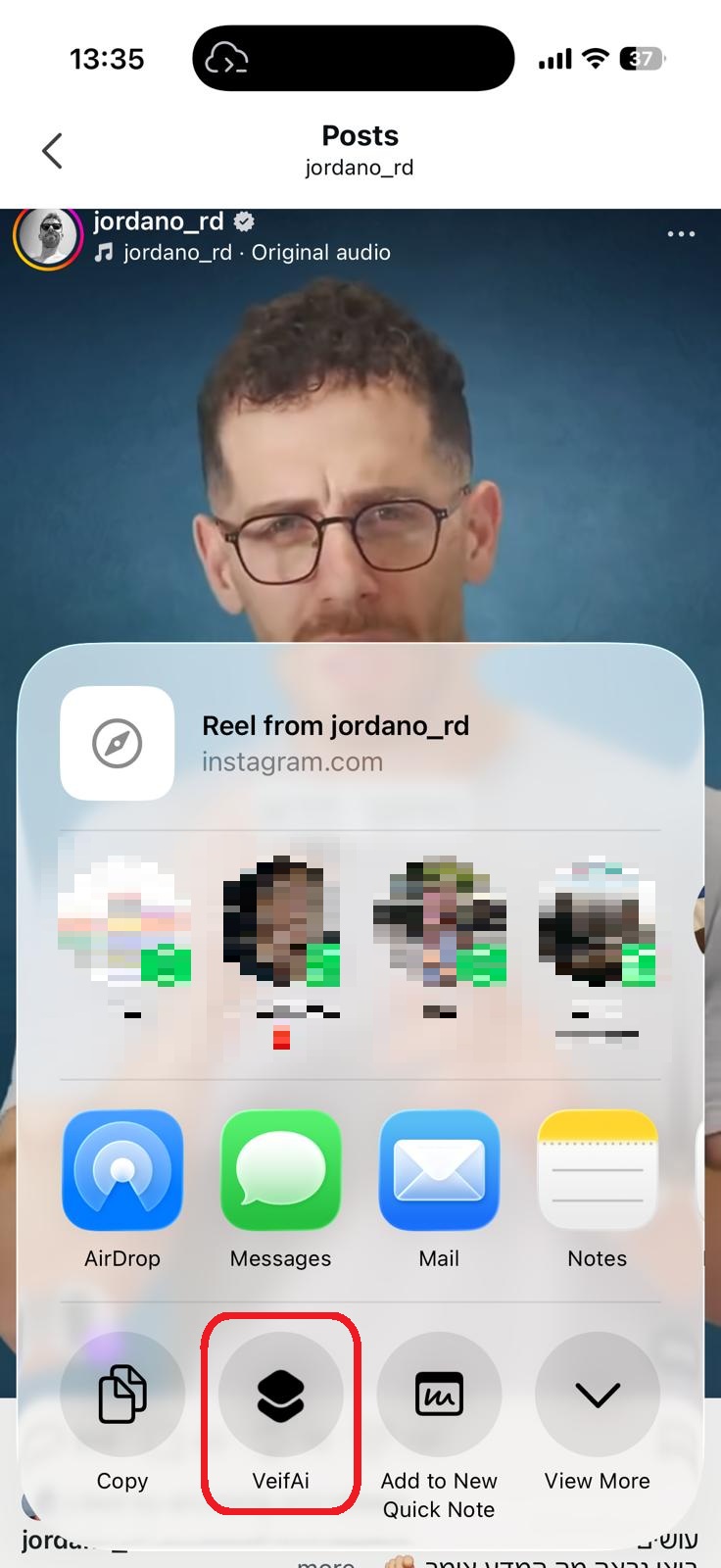
סריקה בתהליך...
הניתוח עשוי לארוך 30–90 שניות
הידעת?
הסרטון אינו מכיל תוכן רפואי
חושבים שחלה טעות?
אם לדעתכם הסרטון אכן עוסק בטענות רפואיות או בריאותיות, הוסיפו הסבר קצר ושלחו בקשה לבדיקה מחדש.
הבקשה התקבלה! נבדוק את הסרטון ונחזור אליכם.
אירעה שגיאה בשליחת הבקשה. נסו שוב.
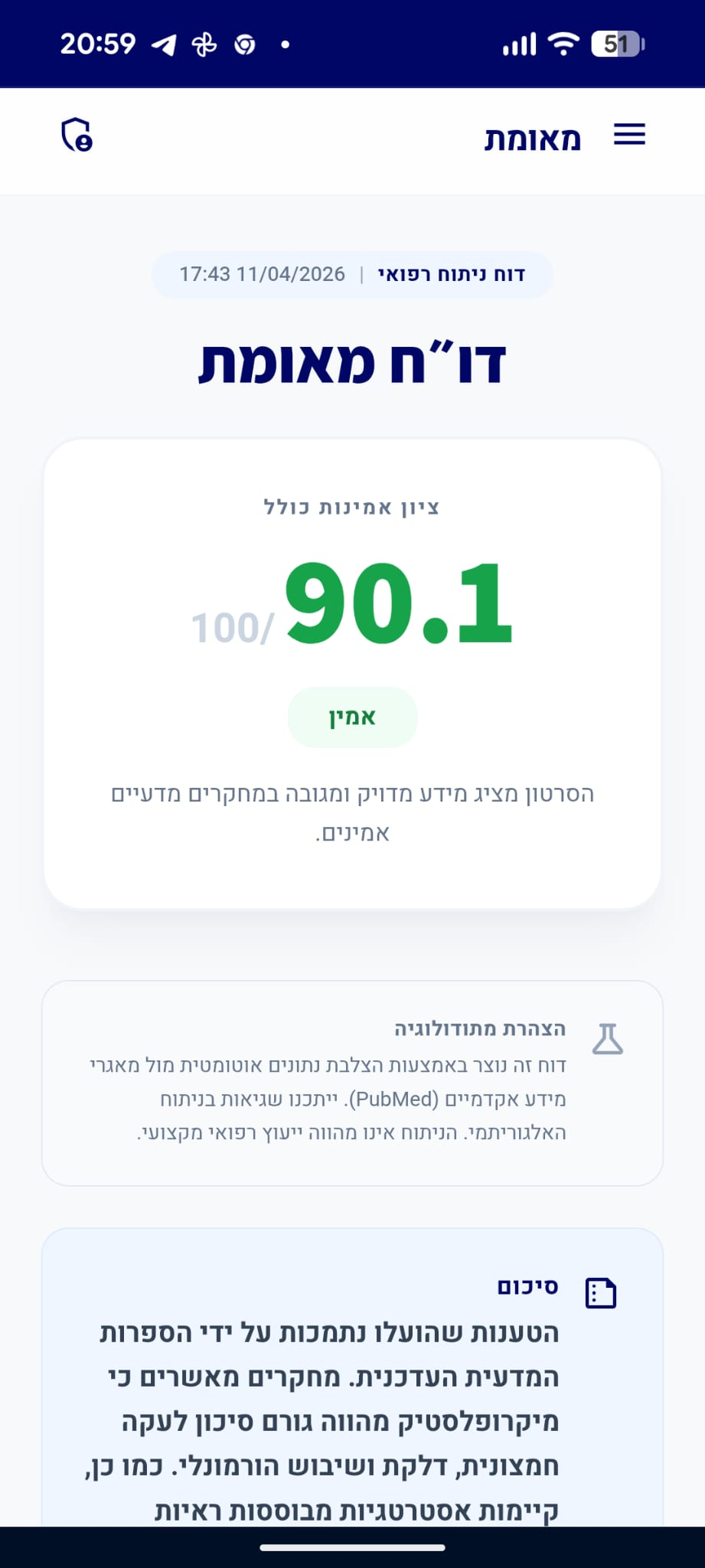
דו״ח מאומת
הסרטון מציג מידע מדויק ומגובה במחקרים מדעיים אמינים.
סיכום
הטענות שהועלו בנוגע למנגנון הפיזיולוגי של הפחתת סוכר בדם באמצעות פעילות גופנית (GLUT4) ולתזמון שיא הסוכר בדם לאחר ארוחה נתמכות על ידי הספרות המדעית. עם זאת, הטענה כי הליכה מיידית לאחר הארוחה עדיפה על הליכה 30 דקות לאחר מכן אינה מגובה בראיות מחקריות חד-משמעיות, שכן מחקרים מצביעים על כך ששני התזמונים יעילים בשיפור בקרת הגלוקוז.
תוכן פרסומי
מקדם: קורס איזון סוכר בשיטה המטבולית (בסרטון)
analytics ניתוח טענות מבוסס ראיות
"הליכה מיד לאחר האוכל יעילה יותר בהפחתת זינוק הסוכר בדם מאשר הליכה 30 דקות לאחר האוכל."
מסקנת הבדיקה:
בעוד שמחקרים מראים כי הליכה לאחר ארוחה מפחיתה את רמות הסוכר בדם בהשוואה למנוחה, לא נמצאה עדות מדעית חד-משמעית לכך שהליכה מיידית יעילה יותר באופן מובהק מהליכה 30 דקות לאחר הארוחה. מחקרים עדכניים מצביעים על כך ששני התזמונים תורמים לשיפור בבקרת הגלוקוז, אך השוואה ישירה ביניהם אינה מראה עליונות מובהקת לאחד על פני השני. (⬜)
"סוכר בדם מגיע לשיאו בין 30 ל-60 דקות לאחר האוכל."
מסקנת הבדיקה:
הספרות הרפואית והנתונים הקליניים מאשרים כי אצל אנשים בריאים, רמות הגלוקוז בדם מגיעות לשיאן בדרך כלל בטווח של 30 עד 60 דקות לאחר צריכת פחמימות, כתלות בהרכב הארוחה ובקצב הפינוי הקיבתי. (🟩)
chevron_right מקורות מדעיים: (2)
-
link
Postprandial glycaemic dips predict appetite and energy intake in healthy individuals.
Understanding how to modulate appetite in humans is key to developing successful weight loss interventions. Here, we showed that postprandial glucose dips 2-3 h after a meal are a better predictor of postprandial self-reported hunger and subsequent energy intake than peak glucose at 0-2 h and glucose incremental area under the blood glucose curve at 0-2 h. We explore the links among postprandial glucose, appetite and subsequent energy intake in 1,070 participants from a UK exploratory and US validation cohort, who consumed 8,624 standardized meals followed by 71,715 ad libitum meals, using continuous glucose monitors to record postprandial glycaemia. For participants eating each of the standardized meals, the average postprandial glucose dip at 2-3 h relative to baseline level predicted an increase in hunger at 2-3 h (r = 0.16, P < 0.001), shorter time until next meal (r = -0.14, P < 0.001), greater energy intake at 3-4 h (r = 0.19, P < 0.001) and greater energy intake at 24 h (r = 0.27, P < 0.001). Results were directionally consistent in the US validation cohort. These data provide a quantitative assessment of the relevance of postprandial glycaemia in appetite and energy intake modulation.…
PMID: 33846643
-
link
A Wavelet AI Algorithm to Automatically Identify Postprandial Glucose Responses From Continuous Glucose Monitoring Profiles in People Without Diabetes.
<h4>Background</h4>Automated identification of postprandial glucose responses (PPGR) from continuous glucose monitoring (CGM) profiles may detect early dysglycemia in people without diabetes. However, no standard approach for this task currently exists.<h4>Methods</h4>We developed a wavelet transform-based AI algorithm to identify PPGRs using only CGM data. The algorithm was evaluated on a public CGM dataset of 25 normoglycemic adults and three independent validation cohorts (n = 65 total) with a mix of normoglycemia and prediabetes. Performance metrics included mealtime prediction error and total and incremental areas under the PPGR curve (tAUC and iAUC, respectively). Associations between AI-derived PPGR parameters and clinical markers such as HbA1c and fasting glucose were also examined.<h4>Results</h4>In the public dataset, 25 participants (age 40 ± 14 years, BMI 26 ± 6 kg/m<sup>2</sup>, HbA1c 5.4 ± 0.4%) provided 3 ± 1 days of paired CGM data and ground-truth mealtimes. The algorithm predicted PPGR start time with a median error of 10 [IQR: 4, 19] minutes relative to ground-truth mealtimes. Postprandial glucose response parameters including tAUC and iAUC derived using ground-truth mealtimes versus AI-predicted mealtime were similar (all <i>P</i> > .1), indicating the algorithm faithfully captured PPGR characteristics. In adjusted analysis, AI-derived PPGR iAUC was independently associated with laboratory markers including HbA1c (β = 0.57 [95% CI: 0.19, 0.95], <i>P</i> = .006) and fasting glucose (β = 0.52 [95% CI: 0.12, 0.92], <i>P</i> = .013). Algorithm performance remained consistent across the three validation cohorts.<h4>Conclusions</h4>The wavelet AI algorithm accurately identified PPGRs from CGM data in people without diabetes, offering a novel automated approach to monitor early signs of postprandial dysglycemia in this population.…
PMID: 41905765
"הליכה מיד לאחר האוכל מסייעת בהכנסת יותר סוכר מהדם לתאי השריר, ובכך מונעת את זינוק הסוכר."
מסקנת הבדיקה:
פעילות גופנית, ובכלל זה הליכה, מעודדת מעבר של נשא הגלוקוז GLUT4 אל קרום התא בשרירי השלד. תהליך זה מאפשר כניסת גלוקוז מהדם אל תוך תאי השריר באופן בלתי תלוי באינסולין, ובכך מסייע בהפחתת רמות הסוכר בדם לאחר ארוחה. (🟩)
chevron_right מקורות מדעיים: (3)
-
link
Altered GLUT1 and GLUT3 gene expression and subcellular redistribution of GLUT4: protein in muscle from patients with acanthosis nigricans and severe insulin resistance.
Multiple isoforms of glucose transporters are found in muscle, the tissue that normally accounts for 85% of insulin-stimulated glucose uptake. Glucose uptake into muscle cells in the fasting state is mediated primarily by GLUT1 and GLUT3 glucose transporters, whereas postprandial (insulin-stimulated) and exercise-related increments in muscle glucose uptake are mediated primarily by GLUT4. To determine if glucose transporters are abnormally expressed in muscle from insulin-resistant subjects, muscle samples were obtained from 10 normal subjects and 6 obese, nondiabetic subjects with severe insulin resistance and acanthosis nigricans. Both GLUT4 total protein and mRNA were normal in the insulin-resistant subjects. Muscle GLUT3 protein and mRNA were lower than controls by 62% and 71%, respectively. GLUT1 mRNA was twice normal, whereas GLUT1 protein content was not significantly increased. GLUT4 protein was markedly redistributed to the muscle plasma membrane in subjects with severe insulin resistance compared with normals (92% v 40% GLUT4 in plasma membrane-enriched fractions, P <.001), whereas the percentage of GLUT1 and GLUT3 protein found in the plasma membrane-enriched fractions was not different from controls. These data document differences in the expression of genes for GLUT1 and GLUT3 in muscle from normal and insulin-resistant subjects. Further, insulin resistance with fasting hyperinsulinemia was associated with a redistribution of GLUT4 to the muscle cell surface with no change in total GLUT4 protein. These data suggest that glucose transporter gene expression and their basal distribution in human muscle are related to insulin resistance and could be determinants of whole body insulin responsiveness.…
PMID: 11436180
-
link
KLF3 impacts insulin sensitivity and glucose uptake in skeletal muscle.
Skeletal muscle is one of the predominant sites involved in glucose disposal, accounting for ∼80% of postprandial glucose uptake, and plays a critical role in maintaining glycemic homeostasis. Dysregulation of energy metabolism in skeletal muscle is involved in developing insulin resistance and type 2 diabetes (T2D). Transcriptomic responses of skeletal muscle to exercise found that the expression of…
PMID: 39250818
-
link
Skeletal muscle metabolism in health and disease: Mechanisms, interventions, and clinical perspectives.
Skeletal muscle is a vital metabolic organ that regulates systemic energy homeostasis by coordinating glucose uptake, fatty acid oxidation, and amino acid metabolism. Its remarkable capacity for dynamic adaptation, termed metabolic flexibility, underpins physical performance and protects against metabolic diseases such as obesity, type 2 diabetes, and sarcopenia. This review provides an integrative synthesis of the molecular and signaling networks that orchestrate skeletal muscle metabolism, focusing on key regulators including insulin, AMPK, mTOR, and PGC-1α. We also examine how disruptions in these pathways lead to mitochondrial dysfunction, lipid dysregulation, and muscle wasting. We explore the therapeutic landscape across pharmacological, exercise-based, and nutritional interventions, emphasizing mitochondrial-targeted strategies and myokine-mediated communication as emerging modalities for restoring metabolic resilience. Additionally, we emphasize the growing importance of multi-omics technologies and inter-tissue communication in improving mechanistic understanding and advancing precision medicine. This review integrates mechanistic, translational, and clinical perspectives to underscore the importance of a systems-level approach to skeletal muscle metabolism. This approach is essential for developing targeted, multidimensional therapies aimed at enhancing metabolic health and extending healthspan.…
PMID: 41858896
videocam הסרטון המנותח
https://www.tiktok.com/@zvikaclinic/video/7625489060819275029/
open_in_newפתח סרטוןהאם הדוח הזה היה מועיל לך?
מה היה פחות טוב? (רשות)
תודה על הפידבק!
עירעור על דוח זה
ספקו ראיות חדשות או הצביעו על אי דיוקים
נעדכן אותך על תוצאות הבדיקה
הוסיפו קישורים למחקרים או מקורות רפואיים מוכרים
העירעור נשלח בהצלחה!
המנוע המדעי שלנו יבדוק את הראיות שהגשתם. נעדכן אתכם באימייל עם התוצאות.
ניתוח מבוסס בינה מלאכותית
דוח זה נוצר באופן אוטומטי על ידי מערכת בינה מלאכותית ועשוי להכיל שגיאות, אי-דיוקים או מידע חלקי. הניתוח אינו מהווה ייעוץ רפואי, אבחנה או המלצה לטיפול, והוא אינו תחליף לדעתו של איש מקצוע רפואי מוסמך. יש להתייעץ עם רופא או מומחה מוסמך לפני קבלת כל החלטה רפואית. המידע מוצג לצרכי מידע כללי בלבד.
מידע זה מופק על ידי בינה מלאכותית ואינו מהווה תחליף לייעוץ רפואי מקצועי.